Los grupos funcionales son responsables de la reactividad y propiedades químicas de los compuestos orgánicos.
sexta-feira, 30 de novembro de 2018
Grupos funcionales
Un grupo funcional es un átomo o un grupo de átomos unidos a una cadena carbonada denominada R, como fórmula general para los compuestos alifáticos y Ar para los compuestos aromáticos.
Los grupos funcionales son responsables de la reactividad y propiedades químicas de los compuestos orgánicos.
Los grupos funcionales son responsables de la reactividad y propiedades químicas de los compuestos orgánicos.
La química del carbono
Por definición un compuesto orgánico es toda sustancia que contiene un átomo de carbono en su molécula. Alguna moléculas aún conteniendo carbono no se consideran compuestos orgánicos, este es el caso de los carbonatos, los carburos y los óxidos simples de carbono. La diferencia es que un un compuesto orgánico, a diferencia de uno inorgánico, cuenta con enlaces carbono-carbono, carbono-hidrógeno o ambos.
Dentro de los enlaces carbono-carbono, distinguimos si cuenta con un enlace simple (alcanos), un enlace doble (alquenos) o un enlace triple (alquinos).
Dentro de los enlaces carbono-carbono, distinguimos si cuenta con un enlace simple (alcanos), un enlace doble (alquenos) o un enlace triple (alquinos).
·Enlace carbono-hidrógeno:
Diferencia entre fluorescencia y fosforescencia
Normalmente, no se suele tener muy clara la diferencia y se usa indistintamente los términos fluorescencia y fosforescencia pero en realidad son procesos distintos.
La fluorescencia es un fenómeno físico a través del cual ciertas sustancias absorben energía a través de luz ultravioleta y la emiten nuevamente en forma de luz, solo que ésta pertenece al espectro visible y tiene un color característico (tiene una longitud de onda determinada). A diferencia del otro, en la fluorescencia, una vez dejas de administrarle esa luz, el proceso se acaba.
La fosforescencia, al contrario, es un proceso más lento en el que las sustancias absorben la energía, almacenándola para luego emitirla en forma de luz o de otra forma de radiación electromagnética.
La fluorescencia es un fenómeno físico a través del cual ciertas sustancias absorben energía a través de luz ultravioleta y la emiten nuevamente en forma de luz, solo que ésta pertenece al espectro visible y tiene un color característico (tiene una longitud de onda determinada). A diferencia del otro, en la fluorescencia, una vez dejas de administrarle esa luz, el proceso se acaba.
La fosforescencia, al contrario, es un proceso más lento en el que las sustancias absorben la energía, almacenándola para luego emitirla en forma de luz o de otra forma de radiación electromagnética.
Para más información haz click aquí.
Daños ocasionados
Aunque la química nos ha ayudado a mejor nuestro modo de vida en muchos aspectos, no podemos olvidarnos de que todas las cosas buenas también tienen sus lados malos, y la química no es una excepción.
Este es un ejemplo de los estragos por la mala gestión de los productos y la carencia de la reutilización:
Mar de plástico
(Mar Mediterráneo)
Por otro lado hay otro tipo de contaminación que aunque no la vemos, está presente y es igual de nociva, como la contaminación del agua por los distintos tipos de vertidos que muchas industrias echan al medio ambiente.
Laboratorios famosos y dónde se encuentran
Laboratorio nacional de Argonne:
Es una de las principales fuentes de Rayos X con un anillo de almacenamiento de electrones.
ALBA- Laboratorio de radiación de Sincrotrón:
Este sincotrón les permite a los científicos españoles estudiar la materia y consta de siete terminales para usos de la radiación.
Edificio Atlas de la Universidad de Wageningen:
Esta universidad pública de los Países Bajos se enfoca sobre todo en los recursos naturales, el medio ambiente y la agricultura.
Laboratorio Nacional Fermi:
El Fermilab, situado en Estados Unidos, cuenta con el segundo acelerador de partículas más potente del mundo después del colisionador de Hadrones. Algunos de los descubrimientos más importantes sobre el modelo de partículas fueron descubiertos allí.
Es una de las principales fuentes de Rayos X con un anillo de almacenamiento de electrones.
ALBA- Laboratorio de radiación de Sincrotrón:
Este sincotrón les permite a los científicos españoles estudiar la materia y consta de siete terminales para usos de la radiación.
Edificio Atlas de la Universidad de Wageningen:
Esta universidad pública de los Países Bajos se enfoca sobre todo en los recursos naturales, el medio ambiente y la agricultura.
Laboratorio Nacional Fermi:
El Fermilab, situado en Estados Unidos, cuenta con el segundo acelerador de partículas más potente del mundo después del colisionador de Hadrones. Algunos de los descubrimientos más importantes sobre el modelo de partículas fueron descubiertos allí.
segunda-feira, 26 de novembro de 2018
Algunos científicos que revolucionaron la química
Lavoisier
Este científico francés del s.XVIII es considerado el padre de la química moderna al haber descubierto la ley de la conservación de la masa. Esta ley consiste en que en una reacción química la suma de la masa de los reactivos tiene que ser igual a la suma de la masa de los productos.
Dalton
John Dalton, químico inglés, elaboró una teoría atómica a partir de la de Rutherford. En ella decía que la materia está compuesta por átomos de distintas masas, que se combinan en proporciones sencillas para formar compuestos.
Mendeléiev
Mendeleiev fue el químico ruso que ideó el sistema de la tabla periódica que empleamos hoy en día. Fue tal su genialidad que a pesar de no tener conocimiento de todos los elementos de los que sí lo tenemos hoy en día, dejó espacios en blanco en la tabla previniendo datos (como la masa atómica) acerca de los elementos que irían ahí colocados. Más tarde se descubrirían y los científicos verían que tenía razón y que las predicciones de éste, eran correctas.

Kekulé
A Kekulé se le considera uno de los fundadores de la teoría estructural de la química y fue el descubridor de la fórmula cíclica del benceno (C6H6) impensable en aquella época, pues se desconocían este tipo de formas en la química orgánica.
Este científico francés del s.XVIII es considerado el padre de la química moderna al haber descubierto la ley de la conservación de la masa. Esta ley consiste en que en una reacción química la suma de la masa de los reactivos tiene que ser igual a la suma de la masa de los productos.
Dalton
John Dalton, químico inglés, elaboró una teoría atómica a partir de la de Rutherford. En ella decía que la materia está compuesta por átomos de distintas masas, que se combinan en proporciones sencillas para formar compuestos.
Mendeléiev
Mendeleiev fue el químico ruso que ideó el sistema de la tabla periódica que empleamos hoy en día. Fue tal su genialidad que a pesar de no tener conocimiento de todos los elementos de los que sí lo tenemos hoy en día, dejó espacios en blanco en la tabla previniendo datos (como la masa atómica) acerca de los elementos que irían ahí colocados. Más tarde se descubrirían y los científicos verían que tenía razón y que las predicciones de éste, eran correctas.

Kekulé
A Kekulé se le considera uno de los fundadores de la teoría estructural de la química y fue el descubridor de la fórmula cíclica del benceno (C6H6) impensable en aquella época, pues se desconocían este tipo de formas en la química orgánica.
sexta-feira, 23 de novembro de 2018
Alquimia 🝳🝮🝤
La Alquimia es un término que viene ya desde la edad media. En esa época se creía que los químicos eran una especie de magos ya que, como es normal, no todas las personas tenían conocimientos acerca de este tema y era incomprensible cómo podían pasar las cosas.
Tiempo más tarde la Alquimia y la Química fueron tomando caminos separados, pues sus fundamentos son distintos. El fundamento de la Alquimia es la creencia de la transmutación de cualquier material en oro. Los alquimistas asignaron unos símbolos a cada uno de los elementos para ellos fundamentales. A continuación encontraréis una imagen con unos pocos. Al igual que en el título de esta publicación, significando cada uno respectivamente:
Tiempo más tarde la Alquimia y la Química fueron tomando caminos separados, pues sus fundamentos son distintos. El fundamento de la Alquimia es la creencia de la transmutación de cualquier material en oro. Los alquimistas asignaron unos símbolos a cada uno de los elementos para ellos fundamentales. A continuación encontraréis una imagen con unos pocos. Al igual que en el título de esta publicación, significando cada uno respectivamente:
Imágenes
quarta-feira, 21 de novembro de 2018
Vídeos
En esta publicación os voy a dejar un par de vídeos de Youtube que considero que son interesantes.
·Indicador de pH, experimento casero:
·Qué ocurre si mezclas Coca-Cola con sal...?
·Experimento con coloides:
·Experimentos variados:
·Pueden una bola de bolos y una pluma caer al mismo tiempo?
(descúbrelo a partir del minuto 2:20)
·Reacción que cambia de color debido a los estados de oxidación del permanganato potásico:
·Reacción con luminol:
domingo, 18 de novembro de 2018
Reacciones
Reacciones de combustión
Las reacciones de combustión siempre se llevan a cabo en presencia de oxígeno. Aunque estamos acostumbrados a ver la llama del fuego en un tono naranja, el color de ésta varía y lo hace en función de la cantidad de energía que desprende. La más energética es la tiene de color azul.
Reacciones nucleares
Llamamos reacción nuclear a aquella que sucede en el núcleo de los átomos. Distinguimos dos tipos: las de fusión, en las que átomos de hidrógeno se fusionan transformándose en helio y liberando una gran cantidad de energía en forma de luz y calor (este tipo de reacción nuclear se dan en las estrellas)
Las reacciones de combustión siempre se llevan a cabo en presencia de oxígeno. Aunque estamos acostumbrados a ver la llama del fuego en un tono naranja, el color de ésta varía y lo hace en función de la cantidad de energía que desprende. La más energética es la tiene de color azul.
Llamamos reacción nuclear a aquella que sucede en el núcleo de los átomos. Distinguimos dos tipos: las de fusión, en las que átomos de hidrógeno se fusionan transformándose en helio y liberando una gran cantidad de energía en forma de luz y calor (este tipo de reacción nuclear se dan en las estrellas)
Reacción de fusión
y las de fisión, en las que los átomos con núcleos inestables se dividen (fisionan) generando energía. Estas reacciones se dan bombas atómicas.
Reacción de fisión
Reacciones de oxirreducción o redox
En este tipo de reacciones hay un cambio de electrones quedando así un elemento oxidado (el que pierde electrones) y el otro reducido (el que los gana). Podemos encontrar este tipo de reacciones en la naturaleza en las plantas al realizar la fotosíntesis.
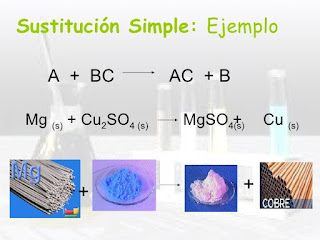
Reacciones de desplazaiento, sustitución o intercambio
En las reacciones de sustitución, un elemento de un compuesto pasa a formar parte del otro debido a su interacción.
Reacciones de doble sustitución
Las de doble sustitución se tratan de unas reacciones similares a las de sustitución simple, a diferencia de las otras, en éstas, dos compuestos intercambian un ión.
Reacciones iónicas
Las reacciones iónicas son producidas ante la exposición de compuestos iónicos a un disolvente. En ellas, el compuesto soluble se disuelve, disociándose en iones.
Reacciones de síntesis o adición
En este tipo de reacciones químicas se combinan dos o más sustancias para formar un único compuesto.
Sabías que...?
·No todas las reacciones desprenden energía de la misma manera. Normalmente asociamos una reacción química con desprendimiento de energía en forma de calor pero éstas también lo pueden hacer en forma de luz. Éste es el caso de las reacciones llevadas a cabo en presencia del luminol.
Reacción con luminol
·La mioglobina es el pigmento responsable del color de la carne roja. Cuanto más mayor sea un animal, más oscura será su carne.
·El timol, presente en el orégano y el tomillo es empleado para la conservación de libros ya que ayuda a la prevención de hongos y de mohos.
·El etileno es un gas natural producido por las frutas y verduras a medida que maduran. Éste ayuda a la maduración de las que se encuentran a su alrededor.
·Las tormentas eléctricas pueden causar reacciones nucleares.
·Dentro de las células de las cebollas hay unos compuestos que contienen azufre. Al cortarlas, estas células se rompen y se transforman en moléculas sulfuradas más volátiles que son liberadas al aire. Al encontrar en contacto y reaccionar con la humedad de tus ojos, estos compuestos sulfurados generando ácido sulfúrico. Una vez tu cerebro detecta la irritación debido a las sensibles terminaciones nerviosas del ojo, responde haciendo que los conductos lacrimales produzcan más agua para así poder disolver el ácido y proteger los ojos.
·En un copo hay aproximadamente 10 elevado a 18 moléculas de agua, las cuales pueden ordenarse en un número casi infinito de formas. A parte de esto, debemos tener en cuenta de que los cristales se forman de distinta forma dependiendo de la tempera. Es por estos motivos que se dice que no existen dos copos de nieve totalmente formados iguales.
Reacción con luminol
·La mioglobina es el pigmento responsable del color de la carne roja. Cuanto más mayor sea un animal, más oscura será su carne.
·El timol, presente en el orégano y el tomillo es empleado para la conservación de libros ya que ayuda a la prevención de hongos y de mohos.
·El etileno es un gas natural producido por las frutas y verduras a medida que maduran. Éste ayuda a la maduración de las que se encuentran a su alrededor.
·Las tormentas eléctricas pueden causar reacciones nucleares.
·Dentro de las células de las cebollas hay unos compuestos que contienen azufre. Al cortarlas, estas células se rompen y se transforman en moléculas sulfuradas más volátiles que son liberadas al aire. Al encontrar en contacto y reaccionar con la humedad de tus ojos, estos compuestos sulfurados generando ácido sulfúrico. Una vez tu cerebro detecta la irritación debido a las sensibles terminaciones nerviosas del ojo, responde haciendo que los conductos lacrimales produzcan más agua para así poder disolver el ácido y proteger los ojos.
·En un copo hay aproximadamente 10 elevado a 18 moléculas de agua, las cuales pueden ordenarse en un número casi infinito de formas. A parte de esto, debemos tener en cuenta de que los cristales se forman de distinta forma dependiendo de la tempera. Es por estos motivos que se dice que no existen dos copos de nieve totalmente formados iguales.
domingo, 11 de novembro de 2018
Enlaces
Los átomos puedes unirse formando enlaces, hay tres tipos:
Covalente: Este tipo de enlace se produce entre átomos no metálicos que comparten un par de electrones, alcanzando con ello estabilidad.

Iónico:El enlace iónico se establece entre un metal y un no metal. En este caso, el átomo no metálico queda con carga negativa al haber captado el electrón del metálico, mientras que este queda con una carga positiva. Se atraen electrostáticamente.

Metálico:Tal como su propio nombre indica, éste es un enlace que se establece entre átomos metálicos. Los núcleos de éstos se encuentran sumergidos en un mar de electrones.

Covalente: Este tipo de enlace se produce entre átomos no metálicos que comparten un par de electrones, alcanzando con ello estabilidad.

Iónico:El enlace iónico se establece entre un metal y un no metal. En este caso, el átomo no metálico queda con carga negativa al haber captado el electrón del metálico, mientras que este queda con una carga positiva. Se atraen electrostáticamente.
Metálico:Tal como su propio nombre indica, éste es un enlace que se establece entre átomos metálicos. Los núcleos de éstos se encuentran sumergidos en un mar de electrones.

Átomo
En esta publicación os voy a dejar una explicación de qué es un átomo e imágenes para que podáis entenderlo mejor.

En la próxima publicación os explicaré los enlaces que forman los átomos.
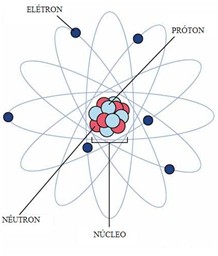
Para empezar a comprender bien la química debemos empezar por lo más básico y fundamental, el átomo.
El átomo es la porción material menor de un elemento químico que interviene en las reacciones químicas y posee las propiedades características de dicho elemento. Este está compuesto a su vez por partículas más pequeñas a las que denominamos partículas subatómicas: En el núcleo se encuentran los protones (con carga positiva) y los neutrones (neutros, sin carga), en la perferia, al rededor de éste se encuentran los electrones (con carga negativa) moviéndose con una elevada velocidad.


En la próxima publicación os explicaré los enlaces que forman los átomos.
quarta-feira, 31 de outubro de 2018
Bienvenidos a mi nuevo blog
Gracias por pasaros por mi nuevo blog. Aquí encontraréis tanto una introducción a la química, como algunas curiosidades de su evolución a lo largo del tiempo.
Día a día ocurren a nuestro alrededor procesos químicos sin que nos demos cuenta.
Mi objetivo principal es que descubráis que la química no es únicamente la teoría que se nos enseña, si no que es algo real y fascinante.
Día a día ocurren a nuestro alrededor procesos químicos sin que nos demos cuenta.
Mi objetivo principal es que descubráis que la química no es únicamente la teoría que se nos enseña, si no que es algo real y fascinante.
"Conocer a la luz del día es juego de niños; en la oscuridad los misterios están en su casa."(Goethe)
Subscrever:
Mensagens (Atom)